| Board | UP Board |
| Textbook | NCERT Based |
| Class | Class 12 |
| Subject | Chemistry |
| Model Paper | Paper 1 |
| Category | UP Board Model Papers |
UP Board Class 12 Chemistry Model Papers Paper 1
समय : 3 घण्टे 15 मिनट
पूर्णांक : 70
निर्देश प्रारम्भ के 15 मिनट परीक्षार्थियों को प्रश्न-पत्र पढ़ने के लिए निर्धारित हैं।
नोट
- इस प्रश्न-पत्र में कुल सात प्रश्न हैं।
- सभी प्रश्न अनिवार्य हैं।
- प्रत्येक प्रश्न के प्रारम्भ में स्पष्ट उल्लेख है, कि उसके कितने खण्ड करने हैं।
- प्रत्येक प्रश्न के अंक उसके सम्मुख अंकित हैं।
- प्रथम प्रश्न से प्रारम्भ कीजिए और अन्त तक करते जाइए। जो प्रश्न न आता हो, उस पर समय नष्ट न करें।
- यदि रफ कार्य के लिए स्थान अपेक्षित है, तो उत्तर-पुस्तिका के बाएँ पृष्ठ पर कीजिए और फिर काट (x) दीजिए। उस पृष्ठ पर कोई हल न कीजिए।
- रचना के प्रश्नों के हल में रचना रेखाएँ न मिटाइए। यदि पूछा गया हो तो रचना के पद अवश्य लिखिए।
- प्रश्न संख्या 1 के अतिरिक्त सभी प्रश्नों के हल के क्रियापद स्पष्ट रूप से लिखिए। प्रश्नों के हल को उत्तर-पुस्तिका के दोनों ओर लिखिए।
- जिन प्रश्नों के हल में चित्र खींचना आवश्यक है, उनमें स्वच्छ एवं स्पष्ट चित्र अवश्य खींचिए। चित्र के बिना हल अशुद्ध तथा अपूर्ण माना जाएगा।
इस प्रश्न के प्रत्येक खण्ड में चार विकल्प दिए गए हैं, सही विकल्प चुनकर उसे अपनी उत्तरपुस्तिका में लिखिए।
प्रश्न 1.
(क) जलीय विलयने में क्षारीय प्रबलता का सही क्रम है।
(a) CH3NH2>(CH3)2NH>(CH3)3N>C6H5NH2
(b) (CH3)3 N>(CH3)2 NH>CH3NH2
(c) (CH3)2NH>(CH3)3NH>CH3NH2
(d) (CH3)2NH>CH3NH2 >(CH3) 3N>C6H NHA
(ख) ऐल्किल हैलाइडों की क्रियाशीलता को घटता हुआ क्रम है।
(a) RI > RCl>RBr
(b) RBr > RCI > RI
(c) RI > RBr > RCI
(d) RCI > RBr > RI
(ग) स्टार्च के जल-अपघटन से बनता है।
(a) ग्लूकोस
(b) फ्रक्टोस
(c) सुक्रोस
(d) माल्टोस
(घ) विलयन जिसमें प्रति लीटर 2.54 ग्राम CuSO4, उपस्थित है, की तुल्यांकी चालकता 91.0 ओम-1 सेमी2 तुल्यांक-1 है। इसकी चालकता होगी
(a) 29 × 10-3 ओम-1 सेमी1
(b) 18 × 10-2 ओम-1 सेमी-1
(c) 24 × 10-3 ओम-1 सेमी-1
(d) 36 × 10-3 ओम-1 सेमी-1
(ङ) संचालित वाहनों के टायर निर्मित होते हैं।
(a) निओप्रीन से
(b) ब्यूना-S से
(c) ब्यूना-N से
(d) प्राकृतिक रबड़ से
(च) nA + mB → उत्पाद, वेग = k [A]n[B]m उपरोक्त अभिक्रिया की कोटि होगी।
(a) n – m
(b) n + m
(c) [latex]\frac { n }{ m } [/latex]
(d) [latex]\frac { m }{ n } [/latex]
प्रश्न 2.
(क) प्रति परासरण क्या है? इसका उपयोग लिखिए। [2]
(ख) 24°C पर एक शर्करा विलयन का परासरण दाब 2.5 वायुमण्डल है। विलयन की सान्द्रता ग्राम मोल प्रति लीटर में ज्ञात कीजिए। [2]
(ग) एक संकुल यौगिक को जब सिल्वर नाइट्रेट के साथ अभिक्रिया कराते हैं, तो सिल्वर क्लोराइड का अवक्षेप प्राप्त होता है। इसके विलयन की मोलर चालकता कुल दो आयनों के संगत होती है। यौगिक का नाम तथा संरचना सूत्र दीजिए।
(घ) थायोसल्फ्यूरिक अम्ल तथा डाइथायोनिक अम्ल की संरचना लिखिए। [2]
प्रश्न 3.
(क) एक fcc संरचना वाले धातु की परमाणवीय त्रिज्या 500 पिकोमी है। इसकी मात्रक कोष्ठिका के किनारे की लम्बाई क्या होगी? [2]
(ख) परमाण्विक कक्षकों में इलेक्ट्रॉनों को भरते समय 3d-कक्षक, 4s-कक्षक से पहले भरी जाती है, परन्तु परमाणु के आयनने के दौरान इसकी बिल्कुल विपरीत होता है। स्पष्ट कीजिए। क्यों? [2]
(ग) थर्मोप्लास्टिक तथा थर्मोसेटिंग बहुलक में क्या अन्तर है? दोनों का एक-एक उदाहरण दीजिए। [2]
(घ) मॉलिश परीक्षण क्या है? यह किस प्रकार किया जाता है? [2]
प्रश्न 4.
(क) ऐमीनो अम्लों की उभयधर्मी प्रकृति का संक्षिप्त वर्णन कीजिए। [3]
(ख) मेथिल ऐमीन अमोनिया से अधिक क्षारकीय है। समझाइए क्यों? [3]
(ग) (i) एन्जाइम की क्रियाविधि को दो पदों में समझाइए।
(ii) रासायनिक समीकरण को पूर्ण कीजिए।
(घ) (i) M2+ आयन (Z = 27) के लिए “चक्रण-मात्र चुम्बकीय आघूर्ण की गणना कीजिए।
(ii) दो लैन्थेनॉइड तत्वों के इलेक्ट्रॉनिक विन्यास लिखकर उनकी ऑक्सीजन अवस्थाएँ भी लिखिए। [3]
प्रश्न 5.
(क)(i) अयस्क तथा खनिजों में अन्तर स्पष्ट कीजिए। [2]
(ii) द्रवस्नेहीं सॉल द्रवविरोधी सॉल की अपेक्षा अधिक स्थायी क्यों होते हैं? [2]
(ख) ऐल्किल हैलाइडों में (C-X) आबन्ध की प्रकृति तथा प्रतिस्थापन अभिक्रियाओं की क्रियाविधि उदाहरण सहित समझाइए। [4]
(ग) (i) ठोस उत्प्रेरकों को चूर्ण रूप में क्यों प्रयुक्त किया जाता है? [2]
(ii) समांगी तथा विषमांगी उत्प्रेरण को उदाहरण द्वारा समझाइए। [2]
(घ) 0.2 ग्राम ऐसीटिक अम्ल के 20.0 ग्राम बेन्जीन में बने विलयन का हिमांक 0.45°C घट जाता है। बेन्जीन में ऐसीटिक अम्ल के द्विलकीकरण की मात्रा की गणना कीजिए।
(बेन्जीन के लिए, Kf = 5.12 केल्विन मोल’ किग्रा) [4]
प्रश्न 6.
(क) (i) पुराने मकान की खिड़कियों के शीशे नीचे से मोटे तथा दूधिया हो जाते हैं, क्यों?
(ii) अक्रिस्टलीय ठोस को परिभाषित कीजिए तथा इसके दो उदाहरण दीजिए।
(iii) 1.00 ग्राम द्रव्यमान के NaCl के घनीय आदर्श क्रिस्टल में कितने इकाई सेल उपस्थित हैं ? [Na = 23, Cl = 355] [5]
अथवा
(i) अणुसंख्य गुणों द्वारा मापन करने पर कुछ विलेय के मोलर द्रव्यमान असामान्य क्यों प्राप्त होते हैं? वाण्ट हॉफ गुणक के आधार पर इसकी व्याख्या कीजिए। [2]
(ii) एक यौगिक के 4,18 ग्राम को 240 ग्राम जल में घोलने पर एक वायुमण्डल दाब पर विलयन का क्वथनांक 100,56°C है। यौगिक के अणुभार की गणना कीजिए।(100 ग्राम जल का आण्विक उन्नयन स्थिरांक K=531 है।) [3]
(ख) (i) कुछ प्राथमिक ऐल्कोहॉलों का ऑक्सीकरण करने पर एस्टर का निर्माण होता है, क्यों? [2]
(ii) एस्टरीकरण की अभिक्रिया लिखिए।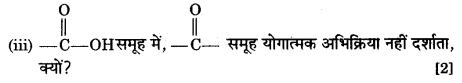
अथवा
(i) निम्नलिखित से ऐसीटोन के निर्माण के लिए रासायनिक समीकरण दीजिए। [2]
(a) द्वितीयक ऐल्कोहॉल से (b) कार्बोक्सिलिक अम्ल से
(ii) स्टीफन अभिक्रिया को समीकरण लिखिए।
(iii) जब साइक्लोहेक्सेन कार्बोल्डिहाइड निम्नलिखित से अभिक्रिया करता है, तो बनने वाला उत्पाद होगा।
(a) PhMgBr तथा H3O+
(b) टॉलेन अभिकर्मक
प्रश्न 7.
(क) (i) ग्रिग्नार्ड अभिकर्मक का उपयोग करते समय नमी के थोड़े अंशों से भी बचना क्यों आवश्यक है? [2]
(ii) निम्नलिखित अभिक्रिया को पूर्ण कीजिए।
अथवा
(i) यौगिक ‘A’ क्षारीय KMnO4 के साथ यौगिक ‘B’ के ऑक्सीकरण द्वारा बनाया गया। यौगिक ‘A’ लीथियम ऐलुमिनियम हाइड्राइड के साथ अपचयन पर वापस यौगिक ‘B’ में परिवर्तित हो जाता है। जब यौगिक ‘A’ को H2SO4 की उपस्थिति में, यौगिक ‘B’ के साथ गर्म करते हैं, तो यह फलों की सुगन्ध वाले यौगिक C को उत्पन्न करता है। यौगिक ‘A’, ‘B’ तथा ‘C’ किस परिवार से सम्बन्धित है?
(ii) निम्नलिखित में कैसे विभेद करेंगे?
फॉर्मिक अम्ल और ऐसीटिक अम्ल [2]
(ख) (i) डेटॉल में पूतिरोधी गुण किस रसायन के कारण होता है? [1]
(ii) ऐस्प्रिन औषधि हृदयाघात से बचाती है। स्पष्ट कीजिए। [2]
अथवा
ऐस्प्रिन एक दर्द में आराम देने वाली ज्वररोधी औषधि है किन्तु दिल के दौरे अर्थात् हृदयाघात रोकने में उपयोग की जा सकती है। समझाइए। [2]
(iii) साबुन की निर्मलन (शोधन) क्रिया मिसेल सिद्धान्त के आधार पर चित्र की सहायता से समझाइए। [2]
अथवा
(i) निम्न घनत्व पॉलिथीन (LDPE) किस प्रकार बनाया जाता है? इसके दो उपयोग लिखिए। [2]
(ii) निम्नलिखित बहुलकों को बनाने वाले एकलकों के नाम लिखिए।
Solutions
उत्तर 1.
(क) (d) +I प्रभाव, संयुग्मी अम्ल के स्थायित्व तथा त्रिविम बाधकता के कारण विभिन्न मेथिल ऐमीनो की क्षारीय प्रबलता का क्रम 20>1″> 3 ऐमीन होता है। अतः सही क्रम निम्न हैं
(CH3)2NH > CH3NH2 > (CH3)3N > C6H5NH2
(ख) (c) R-I आबन्ध की वियोजन ऊर्जा सबसे कम होती है, अतः यह सबसे दुर्बल प्रकृति का होता है। वियोजन ऊर्जा का क्रम
R – Cl > R – Br > R – I है।
अतः क्रियाशीलता का क्रम RI > RBr > RCI है।
(ङ) (b) स्टाइरीन ब्यूटाड़ाइन रबड़ (SBR या ब्यूना -S) का उपयोग संचालित वाहनों के टायर, ट्यूब, आदि बनाने में किया जाता है।
(च) (b) वेग नियम में निहित सभी अभिकारकों की सान्द्रताओं की घातों के योग को उस अभिक्रिया की कोटि कहते हैं।
अतः दी गयी अभिक्रिया की कोटि = n + m होगी
उत्तर 2.
(क) यदि परासरण दाब से अधिक दाब विलयन पर लगाया जाता है, तो विलायक के अणु विलयन (अधिक सान्द्रता) से शुद्ध विलायक (कम सान्द्रता) की ओर प्रवाहित होने लगता है।
चूँकि यह प्रक्रिया, परासरण की क्रिया के विपरीत दिशा में होती है, इसलिए यह क्रिया व्युत्क्रम परासरण कहलाती है। इस प्रक्रम का प्रयोग समुद्री जल प्राप्त करने के लिए तथा घरों में शुद्ध पेयजल प्राप्त करने के लिए किया जाता है।
(ख) दिया है, π = 2.5 वायुमण्डल
T = 24 + 273 = 297 केल्विन
S = 0.0821ली वायुमण्डल डिग्री-1 मोल-1
हम जानते हैं, परासरण दाब, π = CST
या C = [latex]\frac { \pi }{ ST } [/latex] = [latex]\frac { 2.5 }{ 0.0821\times 297 } [/latex] = 0.1025 ग्राम-मोल ली-1
अतः शर्करा विलयन की सान्द्रता 01025 ग्राम मोल ली है।
(ग) AgNO3 के साथ सफेद अवक्षेप का निर्माण दर्शाता है, कि कम से कम एक Cl– आयन समन्वये मंडल के बाहर उपस्थित है। पुनः केवल दो आयन विलयन में प्राप्त होते हैं अतः केवल एक Cl– समन्वय मंडल के बाहर होगा, अतः संकुल का सूत्र [Co(H2O)4Cl2] Cl है तथा इसका नाम टेट्रापेक्वाडाइक्लोरोकोबाल्ट (III) क्लोराइड है।
उत्तर 3.
(क) fee संरचना के लिए, r = [latex]\frac { a }{ 2\sqrt { 2 } } [/latex], a = r × 2√2,
a = 500 × 2√2,
a = 500 × 2 × 1.414
a = 1414 पिकोमी
(ख) n + l नियम कक्षकों में (n + l) मानों के बढ़ते क्रम में इलेक्ट्रॉन भरे जाते हैं अर्थात् उच्च (n+l) मान की अपेक्षाकृत निम्न (n+l) मान वाली कक्षक पहले भरी जाती है।
उदाहरण 3d = n + l = 3 +2 = 5;
4s = n + l = 4 + 0 = 4
अतः इलेक्ट्रॉन 4s-कक्षक में प्रवेश करेगा।
परमाणु के आयनन के लिए आयनन एन्थैल्पी उत्तरदायी है। 4s इलेक्ट्रॉन नाभिक से ढीले बँधे होते हैं, जिस कारण 3d की अपेक्षा 4s से इलेक्ट्रॉन पहले हट जाता है।
(घ) मॉलिश परीक्षण यह कार्बोहाइड्रेट की उपस्थित के विषय में पता लगाने के लिए प्रयुक्त होता है। पदार्थ के जलीय विलयन (2 मिली) में 2 मिली मॉलिश अभिकर्मक (α- नैफ्थॉल का एथिल ऐल्कोहॉल में 10% विलयन) डालो, फिर परखनली को बिना हिलाए बहुत सावधानी से परखनली की दीवार के सहारे बूंद-बूंद करके H2SO4 डालने पर दो पतों के बीच में लाल या भूरे रंग का छल्ला बनता है, जो कुछ समय बाद बैंगनी रंग का हो जाता है, तो काबोहाइड्रेट निश्चित है।
उत्तर 4.
(क) ऐमीनो अम्ल, क्षारीय प्रकृति का ऐमीनो (-NH2) समूह तथा अम्लीय प्रकृति का कार्बोक्सिल (-COOH) समूह रखते हैं। जलीय माध्यम में -NH2 समूह एक प्रोटॉन ग्रहण करता है तथा –COOH समूह एक प्रोटॉन मुक्त करता है। जिसके फलस्वरूप एक द्विध्रुवीय आयतन बनती है, जिसे ज्विटर आयन कहते हैं। इस रूप में ऐमीनो अम्ले, अम्ल तथा क्षार दोनों के समान व्यवहार करता है। अतः ये प्रकृति में उभयधर्मी होते हैं।
(ख) अमोनिया में इलेक्ट्रॉन युग्म रखने वाला नाइट्रोजन परमा तीन हाइड्रोजन परमाणुओं से जुड़ा होता है, जबकि मेथिल ऐमीन में यह एक ऐल्किल समूह भी जुड़ा होता है। ऐल्किल समूह के धनात्मक प्रेरणिक प्रभाव के द्वारा नाइट्रोजन परमाणु के इलेक्ट्रॉन घनत्व में वृद्धि हो जाती है। परिणामस्वरूप मेथिल ऐमीन अमोनिया की तुलना में अधिक सरलता से इलेक्ट्रॉन युग्म का दान कर सकती है। यही कारण है कि मेथिल ऐमीन अमोनिया से अधिक क्षारकीय होती है।
(ग) (i) एन्जाइम की क्रियाविधि निम्न दो पदों में सम्पन्न होती है।
पद I एन्जाइम (E) तथा अभिकारक (S) से मध्यवर्ती संकुल को निर्माण
E+ S →[ES]
पद II [ES] → EP (एन्जाइम उत्पाद जटिल)
EP → E + P (उत्पाद)
यहाँ A = NH3 + Cu2O तथा 200°C व उच्चदाब
B = NaNO2/HCl वे 0-5°C
(घ) (i) 27M = [Ar] 3d74s2
M2+ = [Ar] 3d74s0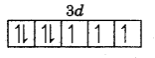
अतः d-कक्षक में इलेक्ट्रॉन भरने पर तीन अयुग्मित इलेक्ट्रॉन प्राप्त होते हैं, अतः n = 3
चुम्बकीय आघूर्ण (µ) = [latex]\sqrt { n(n+2) }[/latex] BM
µ = [latex]\sqrt { 3(3+2) }[/latex] = √15 = 3.87 BM
(ii) लैन्थेनम (57Lu) का इलेक्ट्रॉनिक विन्यास (Xe] 5d1, 6s2 है। यह अपने यौगिकों में + 2 और + 3 ऑक्सीकरण अवस्थाएँ दर्शाता है। सीरियम Ce का इलेक्ट्रॉनिक विन्यास 4f1,5d16s2 है।
इसकी ऑक्सीकरण अवस्था + 1 एवं + 2 हैं।
उत्तर 5.
(क) (i) खनिज अधिकांश धातुएँ प्रकृति में अपने यौगिकों के रूप में अन्य अशुद्धियों के साथ चट्टानों की ऊपरी सतह में पायी जाती हैं, जिन्हें खनिज (Mineral) कहते हैं।
अयस्क वे खनिज जिनसे धातुओं का निष्कर्षण सरल तथा आर्थिक रूप से लाभदायक हो, अयस्क कहलाते हैं। सभी अयस्क खनिज होते हैं। उदाहरण बॉक्साइट (Al2O3 . 2H2O) आदि।
(ii) द्रवस्नेही सॉल अत्यधिक जलयोजित होते हैं तथा जलयोजन के कारण ये अत्यधिक स्थिर होते हैं और सरलता से स्कन्दित नहीं होते हैं। इसके विपरीत द्रवविरोधी सॉल सरलता से स्कन्दित हो जाते हैं, जिसके कारण ये कम स्थायी होते हैं।
(ख) C-X आबन्ध की प्रकृति हैलोऐल्केन में C–X आबन्ध का निर्माण कार्बन के sp3-संकरित कक्षक तथा हैलोजन के np- अपूर्ण कक्षक के अतित्र्यापन द्वारा होता है। चूंकि कार्बन की तुलना में हैलोजन परमाणु अधिक विद्युतऋणात्मक होता है अतः C.-X आबन्ध ध्रुवीय होता है, जिस कारण इनकी क्रियाशीलता उच्च होती है।
C–X आबन्ध की प्रबलता वियोजन ऊर्जा पर निर्भर करती है। इनकी आबन्ध वियोजन ऊर्जा का क्रम C-F>C-Cl>C-Br>C-I होता है।
अत: C-I आबन्ध सबसे दुर्बल प्रकृति का होता है।
जिस कारण नाभिकस्नेही प्रतिस्थापन अभिक्रियाओं में ऐल्किल हैलाइडों, (R-X) की क्रियाशीलता का क्रम इस प्रकार है।
R-I > R—Br > R-Cl > R-F अर्थात् R-I की क्रियाशीलता सबसे अधिक है।
अधिक क्रियाशीलता के कारण ऐल्किल हैलाइड (आयोडाइड) प्रकाश में रखने पर आयोडीन में अपघटित होने के कारण बैंगनी या भूरे रंग के हो जाते हैं।
नाभिकस्नेही प्रतिस्थापन अभिक्रियाएँ
(ग) (i) सामान्यतया ठोस उत्प्रेरकों को चूर्ण रूप में प्रयुक्त किया जाता है, क्योंकि उत्प्रेरक के जितने अधिक टुकड़े होंगे, उतनी ही अधिक मुक्त संयोजकताएँ बढ़ेगी, अर्थात् पृष्ठ क्षेत्रफल बढ़ेगा। इसके फलस्वरूप प्रत्येक की कार्य क्षमता बढ़ती हैं।
(ii) समांगी उत्प्रेरण जब किसी रासायनिक अभिक्रिया में उत्प्रेरक व अभिकारक समान प्रावस्था में होते हैं, तो उत्प्रेरण समांगी उत्प्रेरण कहलाता है।
उदाहरण CH3COOCH3 (aq) + H2O (l) [latex]\underrightarrow { HCl(aq) } [/latex] CH3COOH (aq) + CH3OH (aq)
विषमांगी उत्प्रेरण जब किसी रासायनिक अभिक्रिया में उत्प्रेरक व अभिकारक भिन्न-भिन्न प्रावस्थाओं में होते हैं, तो उत्प्रेरण विषमांगी उत्प्रेरण कहलाता हैं।
N2(g) + 3H2(g) [latex]\underrightarrow { Fe(s) } [/latex] 2NH3 (g)
उत्तर 6.
(क) (i) पुराने मकानों में लगी खिड़कियों के शीशे नीचे से मोटे तथा दूधिया हो जाते हैं, क्योंकि काँच एक छद्म ठोस है तथा गुरुत्व के प्रभाव में मन्द गति से नीचे की ओर बहने लगता है।
(ii) वे ठोस जिनमें अवयवी कणों की कोई निश्चित एवं नियमित व्यवस्था नहीं होती है अर्थात् अवयवी कणों की लघु परासी व्यवस्था पायी जाती है, अक्रिस्टलीय ठोस कहलाते हैं।
जैसे-काँच, रबड़ प्लास्टिक, आदि।
(iii) 1 ग्राम में अणुओं या इकाई सूत्रों की संख्या .
= [latex]\frac { 1 }{ 58.5 } [/latex] × 6.023 × 1023
= 1.029 × 1022
जहाँ, NaCl का सूत्रभार = 23+35.5 = 58.5
इकाई सेल में 4 Na+ आर्यन और 4 Cl– आयन होते हैं।
इकाई सेल = [latex]\frac { { 1029\times 10 }^{ 22 } }{ 4 }[/latex]
= 2.57 × 1021 इकाई सेल
अथवा
(i) कुछ यौगिक (विलेय) विलायकों में घोलने पर अपघटित अथवा संगुणित हो जाते हैं। उदाहरण एथेनॉइक अम्ल के अणुओं का बेन्जीन में हाइड्रोजन आबन्ध बनने के कारण द्वितयन हो जाता है जबकि जल में ये आयन में अपघटित हो जाते हैं। इसके कारण विलयन में रासायनिक स्पीशीज की संख्या, विलयन में मिलाये गये विलेय की रासायनिक स्पीशीज की संख्या की अपेक्षा घट या बढ़ जाती है। चूंकि अणुसंख्य गुणों का मान विलेय के कणों की संख्या पर निर्भर करता है। अतः अणुसंख्य गुणों द्वारा मापन करने पर विलेय का मोलर द्रव्यमान इसके सामान्य मान की अपेक्षा कम या अधिक हो सकता है। इसे ही विलेय का असामान्य मोलर द्रव्यमान कहते हैं। वाण्ट हॉफ ने वियोजन और संयोजन की सीमा के निर्धारण के लिए एक गुणक, i प्रतिपादित किया, जिसे वाण्ट हॉफ गुणक भी कहते हैं।
(ii) प्रश्नानुसार,
यौगिक का भार, w = 4.18 ग्राम
जल का भार, W =240 ग्राम
क्वथनांक में उन्नयन, ΔTb = 100.65 – 100 = 0.65
यौगिक का अणुभार (m) =![]()
Kb = जल का आण्विक उन्नयन स्थिरांक = 5.31
w = यौगिक (विलेय) पदार्थ की मात्रा = 418 ग्राम
W = विलायक (जल) की मात्रा = 240 ग्राम
ΔTb = क्वथनांक में उन्नयन = 065
मान रखने पर, m = [latex]\frac { 1000\times 4.18\times 5.31 }{ 0.65\times 240 } [/latex] = 142.28
(ख) (i) कुछ प्राथमिक ऐल्कोहॉल ऑक्सीकरण पर एस्टर बनाते हैं। ऐसा हेमीऐसीटेल बनने के कारण होता है, जो एस्टर में ऑक्सीकृत हो जाता है।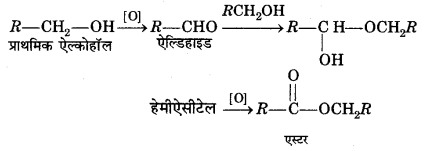
(ii) जब कार्बोक्सिलिक अम्ल सान्द्र H2SO4 की उपस्थिति में ऐल्कोहॉल से क्रिया करता है, तो एस्टर का निर्माण होता है। यह अभिक्रिया एस्टरीकरण कहलाती है।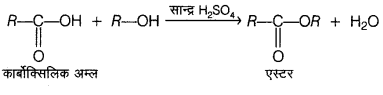


उत्तर 7.
(क) (i) ग्रिग्नार्ड अभिकर्मक एक ध्रुवीय अणु (R-MgX) है। अतः ग्रिग्नार्ड अभिकर्मक अत्यन्त क्रियाशील होते हैं तथा जल (प्रोटॉन का एक उत्तम स्रोत) के साथ क्रिया कर हाइड्रोकार्बनों को देते हैं।
RMgX + H2O → RH + Mg(OH)X
अतः प्रिग्नार्ड अभिकर्मक का उपयोग करते समय नमी के अंशों से बचना चाहिए।
(ii) (a) A = R-CN, B = R-CH2-NH2.(अपचयन)

(ख) (i) डेटॉल में पूतिरोधी गुण क्लोरोजाइलिनॉल के कारण होता है।
(ii) ऐस्प्रिने रक्त स्कन्दनरोधी होती है। इसका उपयोग हृदयाघात को रोकने के लिए भी किया जाता है, क्योंकि यह रक्त स्कन्दन को कम करती है तथा रक्त को तरल करती है। जिससे रक्त सुचारू रूप से शरीर में प्रवाहित होता रहता है और हम हृदयाघात से बच जाते हैं।
(iii) साबुन दीर्घ श्रृंखला वाले वसा अम्लों के सोडियम अथवा पोटैशियम लवण (RCOONa अथवा RC00K) होते हैं। इन्हें जेल में घोलने पर ये आयनित हो जाते हैं।
RCO0Na [latex]\rightleftharpoons[/latex] RCOO– + Na+
पुनः RCOO– दो भाग, लम्बी हाइड्रोकार्बन श्रृंखला R (जलविरोधी) तथा कार्बोक्सिल समूह COO– (जलस्नेही) से मिलकर बना होता है।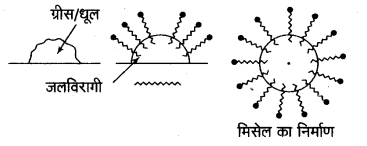
अथवा
(i) 350 से 570 K ताप पर एवं 1000 से 2000 वायुमण्डलीय दाब पर ऑक्सीजन या परॉक्साइड की थोड़ी-सी मात्रा की उपस्थिति में एथीन का बहुलकीकरण कराने पर निम्न घनत्व पॉलिथीन प्राप्त होती है।
यह बहुलकीकरण मुक्त मूलक क्रियाविधि द्वारा सम्पन्न होता है, जिसमें हाइड्रोजन परमाणु का निष्कासन होता है।
इसका उपयोग विद्युत वाहक तारों के विद्युत अवरोधन करने के लिए तथा लचीले पाइप, खिलौने, बोतल, आदि को बनाने में किया जाता है।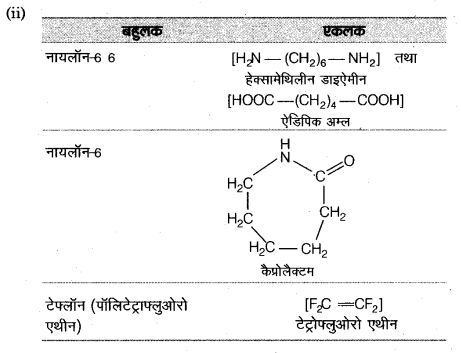
We hope the UP Board Class 12 Chemistry Model Papers Paper 1 download with answers and solutions will help you. If you have any query regarding UP Board Class 12 Chemistry Model Papers Paper 1, drop a comment below and we will get back to you at the earliest.







