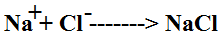CHAPTER -03 [ धातु एवं अधातु ]
CHAPTER-03 PART-01 [NOTES]
WELCOME TO FUTURE ZONE ACADEMY
CLASS 10
Science ch -03 part- 01
#1:- धातु :- वे पदार्थ जो ऊष्मा और विद्युत के सुचालक होते है धातु कहलाते है जैसे :- Fe , Al ,Sn Cu आदि
#2:- अधातु :- वे पदार्थ जो ऊष्मा और विद्युत के कुचालक होता है अधातु कहलाते है जैसे :- रबर , CO2 प्लास्टिक आदि
#3:- धातुओ के गुण :- इनमे निम्न्न्लिखित गुण पाए जाते है –
1:- ये सामन्यत: चमकदार होती है
2:- ये सामन्यत: कठोर और तन्य होती है
3:- ये आघातवर्धनीय होती है
4:- ये ऊष्मा और विद्युत की सुचालक होती है
5:- इनका गलनांक सदैव उच्च होता है
#:- अधतुओ के गुण :- इनमे निम्न्न्लिखित गुण पाए जाते है –
1:- ये सामन्यत: चमकदार नही होती है
2:- ये सामन्यत: कठोर और तन्य नही होती है
3:- ये आघातवर्धनीय नही होती है जबकि भंघुर होती है
4:- ये ऊष्मा और विद्युत की सुचालक नही होती है
5:- इनका गलनांक सदैव निम्न होता है
#4:- धातुओ के रासायनिक गुण :- इनमे निम्न रासायनिक गुण पाए जाते है –
1 :- ऑक्सीजन से अभिक्रिया :- ये ऑक्सीजन से अभिक्रिया करके ऑक्साइड बनाते है अर्थात
धातु + ऑक्सीजन ————–> धातु ऑक्साइड
जैसे :- 2 Mg + O2 ————-> 2MgO
2:- जल से अभिक्रिया :- ये जल से अभिक्रिया करके धातु हाइड्रो ऑक्साइड बनाती है अर्थात
धातु + जल ——————> धातु हाइड्रो ऑक्साइड + हाइड्रोजन
जैसे :- 2Na + 2H2O ———————-> 2NaOH + H2
3:- धातु की अम्ल से अभिक्रिया :- ये अम्ल से अभिक्रिया करके हाइड्रोजन निकालते है अर्थात
धातु + अम्ल —————–> लवण + हाइड्रोजन गैसं
जैसे :- 2Na + 2HCl ——————> 2NaCl + H2
Mg + H2SO4 ———————> MgSO4 + H2
#5:- धातु लवण से अभिक्रिया :- धातु धातु लवण से अभिक्रिया करके कम क्रिया शील धातु को विश्थापित कर देती है
जैसे :- Fe + CuSO4 ————-> FeSO4 + Cu
#6:- सक्रियता श्रेणी :- धातुओ की क्रियाशीलता को अवरोही क्रम में रखने पर बनी श्रेणी सक्रियता श्रेणी कहलाती है कुछ विशेष तत्वों की श्रेणी निम्न है –
Table of Contents
Toggle
#:- सक्रियता श्रेणी के अनुप्रयोग :- इसके निम्नलिखित अनुप्रयोग है –
1:- धातुओ द्वारा जल से हाइड्रोजन गैस को विस्थापित करने की क्षमता ज्ञात करने में
2:- धातुओ की अन्य धातु से विस्थापित करने की क्षमता ज्ञात करने में
3 :- किसी अज्ञात धातु की सक्रियता ज्ञात करने में
CHAPTER-03 PART-02 [NOTES]
WELCOME TO FUTURE ZONE ACADEMY
CLASS 10
Science ch -03 part- 02
वे योगिक आयनिक योगिक होते है जो धातु और अधातु में इलेक्ट्रान के स्थनान्तरण के फलस्वरूप बनते है इन्हें विद्युत संयोजी योगिक भी कहते है जैसे :-
CHAPTER-03 PART-03 [NOTES]
CLASS 10
Science ch -03 part- 03
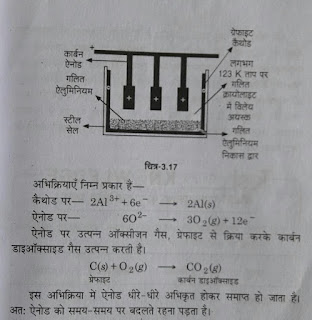
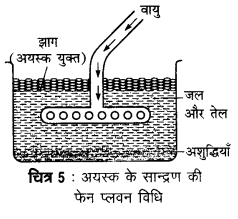
#:- धातुओ के निष्क्रष्ण में निम्नलिखित पद अपनाये जाते है –
| Add caption |
CHAPTER -03 PART-04 [NOTES]
CLASS 10
Science ch -03 part- 04